医薬品等の製造工程において、「GMP」、「バリデーション」という用語が最近
よく使われています。今月は「バリデーション」と計量器の関係について取り上げ
ます。
わが国では薬事法の定めにより、製造販売される医薬品等は厚生労働大臣の
承認を受けなければならないと定められています。そして、その製造販売承認
を取得するための要件として医薬品等の
「製造所における製造管理又は品質
管理の方法が、厚生労働省令で定める基準に適合している」(薬事法第14条)
ことが要求されます。
この省令は「医薬品及び医薬部外品の製造管理及び品質管理の基準に関する
省令」です。また、この省令で定められている医薬品等の製造管理及び品質管理
の基準のことを指して
"GMP"(Good Manufacturing Practice の頭文字)
と称します。
医薬品等は食品と同じく口から体内に摂取したり、血管や皮膚から吸収します。
また、その作用が強いことから、より高い品質を維持することが求められます。
つまり、患者さんが安心して医薬品を使えるために医薬品製造所が定めるべき
管理基準が
"GMP"という訳です。
"GMP"は文書化する必要があります。もういちど省令を参照しますと、次の文書
を作成し保管することが必要とされています。
製品標準書(第7条)
製造管理基準書、品質管理基準書、衛生管理基準書、
製造所からの出荷の管理手順書、変更管理手順書、逸脱管理手順書、
品質等に関する情報及び品質不良等の処理手順書、回収処理手順書、
自己点検手順書、教育訓練手順書、文書及び記録管理手順書、
バリデーション手順書(第8条)
実に多くの文書ですが、
"GMP"の骨子は、ルールを定め文書化し、定められた
手順通りに作業し、結果を記録に残す点にあります。作業者やロットが変わっても、
いつでも同じ品質の医薬品等を製造するために必要な文書です。
さて、文書類の最後にある
"バリデーション"とはどういうことか?について考えま
しょう。
"バリデーション"は少し分かりにくい概念かもしれません。省令によると、
「
"バリデーション"とは、製造所の構造設備並びに手順、工程その他の製造管理
及び品質管理の方法(以下「製造手順等」という。)が期待される結果を与えることを
検証し、これを文書とすることをいう」(第2条)と定義づけられています。分かりにくい
ですね。もともとvalidationという単語が「正当性を実証すること」という意味合いです
ので、
"バリデーション"とは、期待される医薬品等の品質を確保するために、製造
手順等が最適であることを科学的に実証すること、のような理解でよいと考えます。
"バリデーション"の対象は、設備、工程、手順だけではありません。計測機器も
対象です。計量器が適正に使用されないと、期待される医薬品の品質が確保でき
ないからです。
計量器の
"バリデーション"に関しては、次の4つのステップがあると考えられます。
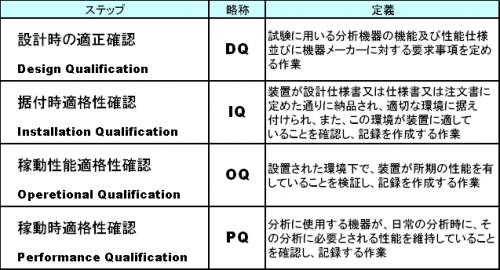
各ステップにおけるクボタの
"バリデーション"に関する考え方は以下の通りです。
(1)まず最初に、
"バリデーション"対応の主体は医薬品製造所(ユーザー様)で
あり、ユーザー様が設計時に作成する適正確認(DQ)の計画に沿うものと考えます。
(2)したがって、クボタとしては、ユーザー様の
"バリデーション"対応への情報提供
にとどめる。提供する情報としては、据付時適格性確認(IQ)シートと稼動性能適格性
確認(OQ)シートの様式の提供、ならびに同シートで参照されることになるドキュメント
(納入仕様書、出荷検査記録等、一部有料です)とします。
(3)IQシート、OQシートの内容はクボタが提供する参考様式である。ユーザー様
がDQにおいて別途計画する場合には適宜ユーザー様にて変更いただくものとします。
(4)稼動時適格性確認(PQ)においては、ユーザー様の日常の点検作業に包含される
ものといたします。このステップでは、決まった質量のものを用いた1点校正で充分であり、
必ずしもトレーサブルな分銅を使用する必要はないと考えるためです。
今月は医薬品等のバリデーションと計量器についてご説明いたしました。
情報提供を行なうIQシート、OQシートについては、1月にクボタWebサイト
にアップする予定ですので是非ご覧ください。
<IQシート>----------------
 <OQシート>----------------
<OQシート>----------------



